In Folge der Arbeiten zur Erfassung und Einstufung von Chemikalien in REACh kann der Hauptbestandteil der klassischen Elektrolyte zur Abscheidung von Chrom sowie notwendige Zusatzstoffe in die Situation geraten, nur noch in sehr beschränktem Maße einsetzbar zu sein. Als Alternative kommen Elektrolyte auf Basis von Chrom(III)verbindungen in Betracht. Verfügbar sind hierfür derzeit Verfahren zur Abscheidung von dekorativen und dünnen Glanzchromschichten. Deren Einsatz erfordert einen höheren Aufwand in Bezug auf den sorgfältigen Umgang mit den Elektrolyten und die Vermeidung des Eintrags von Fremdstoffen. Erste Erfahrungen mit großen Volumina zeigen positive Ergebnisse.
Chromium Electrodeposition from Trivalent Electrolytes
A consequence of the assessment of the chemicals involved and their classification under the EU REACh Directive is that hexavalent chromium salts, the main constituent involved, as well as various additives, can now no longer be used except in extremely limited circumstances. The alternative is to use electrolytes based on trivalent chromium. At present, these electrolytes can only be used for electrodeposition of decorative chromium plating and relatively thin bright deposits. Such systems are more demanding in terms of electrolyte maintenance and avoiding contamination with foreign species. Initial experiences using large volumes have provided very positive results.
1 Einführung
Die Glanzchromabscheidung ist ein wesentlicher Verfahrensschritt in der dekorativen Veredlung einer Vielzahl von Gegenständen des Alltags. Verchromten Oberflächen begegnet man zum Beispiel bei Sanitärgegenständen, dekorativen Oberflächen im Automobilbereich, bei Ladeneinrichtungen oder Personenleitsystemen in vielen Bereichen des öffentlichen Lebens, um nur einige der markantesten Anwendungen aufzuzählen. Die dekorative Glanzverchromung erfolgt noch zum überwiegenden Teil aus den traditionellen Elektrolyten auf Chromsäurebasis, das heißt der Verbindung mit sechswertigen Chromionen. Verfahren auf der Basis dreiwertiger Chromverbindungen sind seit etwa 1970 bekannt und auch im Einsatz. Der Anteil am Gesamtvolumen der Verchromungselektrolyte war bisher relativ gering, auf die dafür verantwortlichen Gründe wird später eingegangen werden.
2 Abscheidung aus Chromsäure
Klassische Chromelektrolyte auf Basis von Chromsäure (H2CrO4) enthalten diese im Konzentrationsbereich von etwa 125 g/l bis 300 g/l. Chromsäure und Chromate sind nach der Gefahrstoffverordnung als T+ (sehr giftig) eingestuft. Beim Betrieb solcher Verfahren müssen entsprechende Sicherheitsmaßnahmen eingehalten werden, um eine Gefährdung von Mensch und Umwelt ausschließen zu können. Trotz der hohen Giftigkeit von Chromaten ist der Umgang beherrschbar. Nach Anhang 40 der Verordnung über Anforderungen an das Einleiten von Abwasser in Gewässer gilt ein Grenzwert von 0,1 mg/l Chrom(VI) im Abwasser. Dieser kann von den Betreibern eingehalten werden, wie durch Eigenüberwachungen und auch behördlich beauftragte Abwasseruntersuchungen belegt werden kann.
Die Verwendung von Chromsäure wird durch gesetzliche Vorgaben zunehmend erschwert. Zu nennen ist hier zum Beispiel die Störfallverordnung (12. BImSchV) von 2005. Mit der genannten Konzentration an Chromsäure sind auch die fertig angesetzten Elektrolyte als sehr giftig (T+) einzustufen. Der Galvanikbetrieb fällt dann unter die Pflichten der Störfallverordnung, wenn die Mengenschwelle von 5000 kg erreicht oder überschritten wird. Ab 20 000 kg gelten dann zusätzlich noch die erweiterten Pflichten nach § 9–12 der Störfallverordnung.
Der Wirkungsgrad der Chromelektrolyte liegt bei maximal 25 %. Der restliche Strom führt zu Wasserstoffentwicklung, verbunden mit starker Aerosolbildung. Diese Chromsäureaerosole sind nach der Verordnung 1272/2008/EG mit H330 (Lebensgefahr beim Einatmen) eingestuft. Nach der Richtlinie 1999/45/EWG galt die Einstufung R26 (sehr giftig beim Einatmen). Die Aerosolbildung konnte durch den Einsatz von perfluorierten Tensiden, besonders das Perfluoroctansulfonat (PFOS), soweit unterdrückt werden, dass keine Gefahren für das Bedienungspersonal und die Umwelt zu befürchten waren. Allerdings sind die Perfluoroctansulfonate chemisch so beständig, dass sie weder im Chromelektrolyten noch später in der Umwelt nennenswert abgebaut werden. In der Folge davon kommt es zu einer Anreicherung in Flüssen und Gewässern. Sie gelangen somit in die Nahrungskette. Der Einsatz bei der Verchromung ist daher nur noch unter bestimmten Auflagen zulässig.
Es wurden intensive Anstrengungen unternommen, um geeignete Alternativen zu den Perfluoroctansulfonaten zu entwickeln. Chromsäureelektrolyte wirken stark oxidierend. Nicht fluorierte Verbindungen werden chemisch abgebaut. In den meisten Fällen verbleiben teerartige Rückstände als Abbauprodukte, die sich auf die zu verchromenden Oberflächen auflegen und somit keine fehlerfreie Verchromung mehr ermöglichen. Organische Verbindungen, die im Chromelektrolyten stabil sind und chemisch nicht verändert werden, sind dann aber zwangsläufig auch in der Umwelt unter wesentlich milderen Bedingungen stabil und werden nicht abgebaut. Eine Anreichung in der Umwelt ähnlich zu den Perfluoroctansulfonaten kann somit nicht ausgeschlossen werden. Das eigentliche Ziel bei der Substitution der Perfluoroctansulfonate wäre somit noch nicht erreicht.
Die Aufnahme von Chromsäure in den Anhang XIV der REACh-Verordnung am 17. April 2013 baute weitere Hürden für die Verwendung dieses Stoffes auf. Ohne Beantragung einer Zulassung für die Glanzchromabscheidung darf dieser Stoff nach dem 21. September 2017 nicht mehr verwendet werden. Auch wenn mit der Beantragung einer Zulassung begonnen wurde und weitere rechtliche Schritte eingeleitet wurden, ist deren Ausgang unsicher. Und auch bei einer Zulassungserteilung muss berücksichtigt werden, dass diese nicht auf unbestimmte Dauer erteilt wird, sondern nach Artikel 60 der REACh-Verordnung einer befristeten Überwachung unterliegt.
3 Abscheidung aus Chrom(III)-verbindungen
Vor dem Hintergrund dieser Hürden, die für die Anwendung von Chromsäure für die Verwendung zur Glanzchromabscheidung aufgebaut wurden, rücken Verfahren auf der Basis von dreiwertigen Chromverbindungen wieder stärker in das Interesse der Anwender. Obwohl diese Verfahren seit etwa 1970 bekannt sind, war die Anwendung bisher nur wenig verbreitet. Bei den Verfahren auf Chloridbasis konnte der gewohnte helle Chromglanz der konventionellen Chromelektrolyte nicht erreicht werden. Das stellt insbesondere für einen Auftraggeber, der Bauteile bei verschiedenen Galvanikunternehmen beschichten lässt, ein großes Problem dar. Bauteile aus klassischen Chromsäureelektrolyten können nicht mit solchen aus dreiwertigen, chloridhaltigen Elektrolyten verbaut werden. Der Farbunterschied der einzelnen Oberflächen wäre zu groß. Erschwerend kommt hinzu, dass Chrom(III)-elektrolyte sehr empfindlich gegen Metallverunreinigungen wie Zink, Kupfer, Nickel und Eisen reagieren (Tab. 1). Ein Überschreiten der Grenzwerte führt zu dunkleren Schichten oder weiteren Abscheidungsfehlern, wie beispielsweise zu Deckungsproblemen.

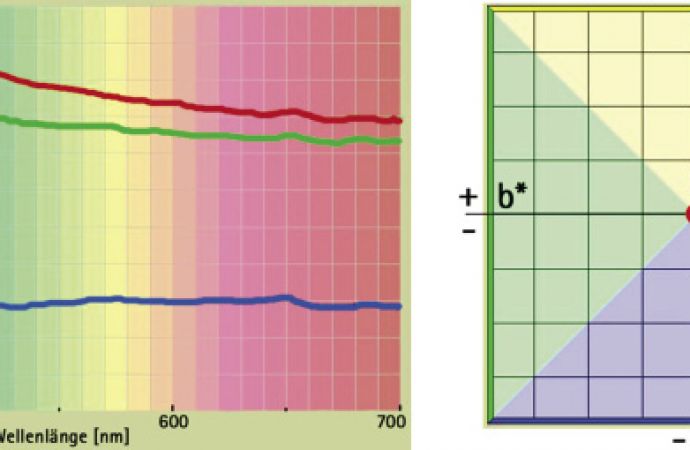
Die Entwicklung von Chromelektrolyten auf Basis von Chrom(III)sulfat führte zu einer wesentlichen Verbesserung der Abscheidung. Die Dr.-Ing. Max Schlötter GmbH & Co. KG brachte 2008 das sulfathaltige Verfahren Slotochrom DR 60 auf den Markt. Die Anforderungen an die Optik der Schichten konnten erfüllt werden. Die farblichen Unterschiede zwischen einer Chromschicht aus einem Chromsäureelektrolyten und dem Chrom(III)elektrolyten Slotochrom DR 60 oder in der Weiterentwicklung dem Slotochrom DR 1140 sind kaum noch wahrnehmbar, wie durch Farbmessungen gezeigt werden konnte (Abb. 1).

Abb. 1: Farbmessung von Chromschichten; rot: Chromschicht aus Chrom(VI)elektrolyt; grün: Chromschicht aus Chrom(III)elektrolyt, Chrombad Slotochrom DR 1140, Sulfatbasis; blau: Chromschicht aus Chrom(III)elektrolyt, Chrombad Slotochrom DR 60, Chloridbasis
Wie bei jedem neuen Verfahren blieb es nicht aus, dass sich im praktischen Betrieb Störungen einstellten, die so in der Entwicklungsphase des Verfahrens nicht in vollem Umfang erkannt werden konnten. Ähnlich wie die chloridhaltigen Verfahren sind auch die sulfathaltigen, dreiwertigen Chromelektrolyte empfindlich gegen Metallverunreinigungen. Bei sorgfältiger Prozessführung sind die Grenzwerte jedoch sicher einhaltbar beziehungsweise die Fremdmetalle lassen sich durch Einsatz eines speziellen Fällungsmittels in einfacher Weise abtrennen. Da die zu verchromenden Teile immer aus einem vorgeschalteten Nickelelektrolyten kommen, ist eine gute Spültechnik Voraussetzung, um Verunreinigungen durch Nickel im Chromelektrolyten zu minimieren.
Störungen bei der Abscheidung werden auch durch Chromate ab Konzentrationen von etwa 50 mg/l verursacht. Es kommt hier insbesondere zu Deckungsproblemen. Chrom(VI)verbindungen können durch Oxidation der Chrom(III)verbindungen an der Anode entstehen. Zum Einsatz kommen bei den sulfathaltigen Chromelektrolyten bevorzugt mit Mischmetalloxiden beschichtete Titanmaterialien (Streckmetallgitter oder vollflächiges Material). Die Beschichtung besteht in der Regel aus Iridium- und Tantaloxiden. Trotz nominal gleicher Zusammensetzung wurden erhebliche Unterschiede im Ausmaß der Chrom(VI)bildung im laufenden Betrieb festgestellt. Eine sorgfältige Auswahl der geeigneten Anoden ist daher für die störungsfreie Arbeitsweise von hoher Wichtigkeit.
Die hohe Empfindlichkeit von Chrom(III)-elektrolyten gegen Verunreinigungen durch sechswertiges Chrom ist auch bei der Installation eines solchen Elektrolyten zu berücksichtigen. Ein einfaches Austauschen des Chromsäureelektrolyten in einer bestehenden Anlage durch einen Chrom(III)elektrolyten ist nicht möglich. Ein Behälter, der zuvor einen Chromsäureelektrolyten enthielt, lässt sich niemals so sauber spülen, dass im späteren Kontakt mit dem Chrom(III)-elektrolyten nicht doch noch Reste von Chrom(VI)verbindungen ausgelaugt würden. Ähnlich verhält es sich mit Rohrleitungen. Hier ist ein entsprechender Austausch der Anlagenteile erforderlich; beim Wannenbehälter muss mindestens ein entsprechender Inliner – eine eingelegte Schutzhülle ohne tragende Funktion – vorgesehen werden. Die hier angesprochenen Parameter sind in Tabelle 2 in einer Übersicht dargestellt.

3.1 Energieverbrauch bei der Chromabscheidung
Die Stromkosten bei der Chromabscheidung setzen sich im Wesentlichen aus der Elektrolytspannung, der kathodischen Stromausbeute und der Anzahl der zu übertragenden Elektronen zusammen. Bezüglich des letzten Punktes ist die Abscheidung aus den dreiwertigen Chromelektrolyten zunächst im Vorteil, da für die gleiche Schichtdicke an Chrom nur die halbe Ladungsmenge übertragen werden muss.
Für die Arbeitsspannung ist die elektrische Leitfähigkeit des Elektrolyten die entscheidende Größe. Chrom(III)elektrolyte arbeiten in einem pH-Bereich von etwa pH 3,5 bis pH 4. Der elektrische Strom wird im Elektrolyten durch die Kationen und Anionen des Leitsalzes und in untergeordnetem Maße von den Chromsalzen bewirkt. Bei einer Elektrolyttemperatur von 50 °C liegt die elektrische Leitfähigkeit eines Chrom(III)-elektrolyten bei etwa 100 mS/cm. Sie ist damit etwa doppelt so hoch wie die eines typischen Watts-Nickelelektrolyten mit 40 mS/cm bis 50 mS/cm. In Chromsäureelektrolyten erfolgt der Ladungstransport durch die Wasserstoffionen (H+), die eine wesentliche höhere Äquivalentleitfähigkeit besitzen als Metallionen. Die Leitfähigkeit eines typischen Chromsäureelektrolyten mit etwa 200 g/l Chromsäure erreicht bei einer Elektrolyttemperatur von 50 °C einen Wert von 500 mS/cm bis 600 mS/cm und ist damit um den Faktor 5 bis 6 höher als die eines Chrom(III)elektrolyten [1].
Aufgrund dieser Überlegung erscheint zunächst der Energieaufwand bei einem Chromsäureelektrolyten geringer zu sein, als der bei einem Chrom(III)elektrolyten. In der Summe aller Parameter ergibt sich aber doch ein Vorteil für Chrom(III)elektrolyte. Die Abscheidung aus Chromsäureelektrolyten erfolgt üblicherweise bei kathodischen Stromdichten von 15 A/dm2, aus Chrom(III)-elektrolyten bei 5 A/dm2. Bei vergleichbaren Expositionszeiten von etwa fünf Minuten für die erforderliche Schichtdicke ergibt sich aus dem Produkt von Strom und Spannung eine deutlich niedrigere elektrische Leistung für den Chrom(III)elektrolyten, wenn bei vergleichbaren Abscheidespannungen gearbeitet werden kann.
3.2 Neue Elektrolytvarianten in der Anwendung
Die Erfahrungen beim Einsatz des Chrombades Slotochrom DR 60 in der Praxis wurden gesammelt und flossen in die Weiterentwicklung des Verfahrens ein. Die zweite Generation wurde schließlich unter dem neuen Verfahrensnamen Slotochrom DR 1140 im zweiten Quartal 2013 auf den Markt gebracht. Mittlerweile wird bei einem Großkunden die gesamte zu verchromende Ware im Chrombad Slotochrom DR 1140 bearbeitet. Das Gesamtvolumen der Chromelektrolyte in zwei Anlagen bei diesem Anwender beträgt etwa 50 000 Liter.
Während ein Chrom(III)elektrolyt auf Chloridbasis ohne organische Zusätze betrieben wird, benötigt ein Verfahren auf Sulfatbasis spezielle organische Additive. Diese haben jeweils eigene Funktionen. Sie sind so beispielsweise verantwortlich für Farbe, Glanz, Deckfähigkeit und Schichtdicke. Da die Substanzen in ihrer Wirkung zum Teil in Wechselwirkung treten können, ist eine genaue Abstimmung der Dosierung erforderlich. Das Zusatzsystem für das System Slotochrom DR 1140 wurde so konzipiert, dass zum Beispiel die erreichbare Schichtdicke reproduzierbar über die Konzentration einer im Elektrolyten analytisch überwachbaren Komponente gesteuert werden kann. Das Fine-Tuning der Elektrolyteinstellung gelingt am Anfang am einfachsten, wenn mit Einzelkomponenten dosiert werden kann. Sobald jedoch genügend Erfahrungswerte bezogen auf die anlagentechnischen und artikelspezifischen Parameter vorliegen, lässt sich die Elektrolytführung durch Mischen der Einzelzusätze im richtigen Verhältnis zu Ergänzungslösungen vereinfachen.
4 Systemvergleich
Bei allen Bemühungen, den Schichteigenschaften der aus Chromsäure- beziehungsweise Chrom(III)elektrolyten abgeschiedenen Schichten so nahe wie möglich zu kommen, bleibt ein prinzipieller Unterschied bestehen. In Chromsäureelektrolyten bewirkt die Chromsäure eine Passivierung nicht beschichteter Oberflächen, zum Beispiel die Innenflächen von Stahlrohren. Chrom(III)elektrolyte können eine solche Passivierung nicht erzeugen. Die Oberflächen kommen hochaktiv aus dem Elektrolyten. Im Innenbereich von Stahlrohren kann sich daher sehr leicht Flugrost ausbilden. Man könnte hier zwar einen Schritt rückwärts machen und zur Passivierung eine Nachtauchung in einer Chromsäurelösung vornehmen. Die notwendige Konzentration der Lösung kann zwar deutlich unter der eines konventionellen Chromelektrolyten liegen, dennoch würde eine solche Maßnahme das Ziel einer Substitution von Chromsäure in der Produktion unterlaufen. Schlötter hat für diese Anwendung das chromfreie Verfahren Slotoprotect FE 1050 entwickelt. Es erzeugt einen temporären Korrosionsschutz auf Eisenwerkstoffen und verhindert die Flugrostbildung.
4.1 Korrosionsbeständigkeit
Eine vergleichende Prüfung von Produktionsbauteilen wurde nach der Norm DIN EN ISO 6270-2 durchgeführt. Eine Beständigkeit von 20 Zyklen wurde bei allen Prüflingen aus Chrom(III)- und Chrom(VI)-
elektrolyten ohne Probleme erreicht.
Bei vergleichenden Prüfungen nach Norm DIN EN 9227 weisen Beschichtungen aus Chrom(III)elektrolyten eine tendenziell etwas schlechtere Beständigkeit auf. Hier ist auf eine ausreichende Schichtdicke der Nickelschicht zu achten. Bei zu dünnen Nickelschichten und eventuell noch vorhandenen Poren in der Nickelschicht wirkt sich die fehlende Passivierung der Schichten im Chrom(III)elektrolyten nachteilig aus. Wenn Mindestschichtdicken von etwa 20 µm bei der Nickelabscheidung eingehalten werden, sind keine Unterschiede mehr in der Korrosionsbeständigkeit feststellbar (Tab. 3).

5 Elektrolytaufbau und Funktion
Nachfolgend sind die wesentlichen Komponenten des Chromelektrolyten Slotochrom DR 1140 und deren Funktion beziehungsweise Wirkung zusammengestellt.
- Das Leitsalz Slotochrom DR wird in einer Konzentration von 200 g/l bis 230 g/l eingesetzt und sorgt für die notwendige elektrische Leitfähigkeit des Elektrolyten.
- Die Borsäurekonzentration beträgt 45 g/l bis 55 g/l. Neben der Pufferwirkung hat Borsäure auch eine katalytische Funktion und ermöglicht, dass es überhaupt zu einer geschlossenen Chromabscheidung kommt.
- Die Chromlösung Slotochrom DR enthält dreiwertige Chromsalze und einen schwachen Komplexbildner. Die Lösung wird zum Ansetzen des Elektrolyten und für die laufende Ergänzung des Chromgehalts während der Abscheidung verwendet.
- Die Zusätze Slotochrom DR 1141 und Slotochrom DR 1142 sind die eigentlichen Glanzbildner im Elektrolyten und sind für die typische Chromfarbe der abgeschiedenen Schicht verantwortlich.
- Der Zusatz Slotochrom DR 1144 bewirkt als Katalysator, dass die Chromschicht mit der gewünschten Schichtdicke abgeschieden werden kann. Der Zusatz kann im Elektrolyten analytisch bestimmt werden. In der Praxis ist es jedoch ausreichend, wenn die Konzentration indirekt über die Messung der abgeschiedenen Schichtdicke bestimmt wird. Wenn die Schichtdicke zu niedrig ist, kann eine Korrektur durch Zugabe von Zusatz Slotochrom DR 1144 in Schritten von 0,1 ml/l erfolgen. Bei Schichtdicken über 0,3 µm kann es jedoch zu deutlich wahrnehmbaren Schleiern kommen.
- Das Netzmittel Slotochrom DR 1146 verhindert Porenbildung im Überzug durch anhaftende Wasserstoffbläschen. Darüber hinaus kann es als Sonderkorrektur beim Auftreten von Schleiern oder Schlieren in der Schicht zugegeben werden.
Der Elektrolyt Slotochrom DR 1140 zur Abscheidung von glänzenden Schichten wird mit Warenbewegung betrieben. Diese kann durch eine schwache Lufteinblasung unterstützt werden. Eine kräftige Luftbewegung sollte trotzdem vorgesehen werden, falls der Elektrolyt während der Arbeitspausen auf Temperaturen unterhalb des Arbeitsbereichs abkühlt. Im Interesse einer möglichst hohen elektrischen Leitfähigkeit wird der Elektrolyt mit einer hohen Leitsalzkonzentration betrieben. Bei einem deutlichen Unterschreiten der empfohlenen Elektrolyttemperatur kann es daher zum Auskristallisieren der gelösten Salze kommen. Eine intensive Luftbewegung unterstützt in der Phase der Wiederinbetriebnahme deren Rücklösen. Die zur Elektrolytbewegung verwendete Luft muss öl- und staubfrei sein. Abhängig vom Warenspektrum kann auch eine Elektrolytbewegung mittels Eduktoren (Venturidüsen) zweckmäßig sein.
In Tabelle 4 sind alle Bestandteile mit den optimalen Gehalten im Elektrolyten sowie die wichtigsten Arbeitsparameter zusammengestellt.

Literatur
[1] G. A. Lausmann, J. N. Unruh: Die galvanische Verchromung; 2. Auflage, Eugen G. Leuze Verlag, 2006, Seite 162
DOI: 10.7395/2013/Jordan1