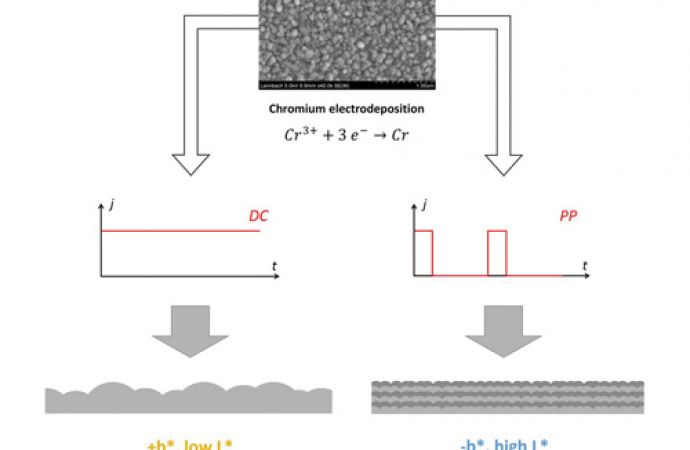
zur Anpassung des optischen Erscheinungsbilds
Das optische Erscheinungsbild von galvanisch abgeschiedenen Chromschichten ist eines der wichtigsten Kriterien für deren dekorative Anwendung. Für die dekorative Verchromung werden zunehmend Elektrolyte auf Basis von dreiwertigem Chrom als Ersatz für die bisher verwendeten Elektrolyte auf Basis von sechswertigem Chrom eingesetzt. Chrom aus Elektrolyten mit dreiwertigen Chromverbindungen neigt jedoch dazu, bei Dicken über 100 nm einen gelblichen Farbton zu haben, was für die meisten Anwendungen unerwünscht ist. Die Farbverschiebung hängt mit einer Änderung der Oberflächenmorphologie aufgrund des Wachstums der Chromkeime zusammen. Durch die Verwendung von gepulstem Strom mit Einschaltzeiten im Bereich von Sekunden wird das unerwünschte Kornwachstum unterdrückt und die Bildung frischer Kerne begünstigt. Dadurch bilden sich kompakte Chromschichten mit feinerem Gefüge und verbesserten Farbwerten. Ein bläuliches Aussehen und ein hoher Glanz werden bis zu einer Dicke von mehr als 200 nm beibehalten. Basierend auf den Ergebnissen wird eine Kombination aus konstantem und gepulstem Strom vorgeschlagen, die ein ähnliches visuelles Erscheinungsbild ergibt wie nur bei gepulstem Strom, jedoch die angestrebte Schichtdicke in deutlich kürzerer Zeit erreicht.
Hinweis
Der vorliegende Artikel wurde in der Erstfassung im Journal of Applied Electrochemistry in englischer Sprache veröffentlicht unter der folgenden Bezeichnung: M. Leimbach, Chr. Tschaar, U. Schmidt, A. Bund: Low-frequency pulse plating for tailoring the optical appearance of chromium layers for decorative applications; Journal of Applied Electrochemistry, 50 (2020), p. 489–499, http://doi.org/10.1007/s10800-020-01406-3
1 Einleitung
Die galvanische Abscheidung von Chrom für dekorative Anwendungen spielt in der Oberflächenveredelungsindustrie eine herausragende Rolle, insbesondere in den Industriebereichen Sanitär, Automobil, Ladenbau, Haushaltswaren oder Beschichtung von Kunststoffen (um nur die wichtigsten zu nennen) [1]. Bei diesen Anwendungen sind Chromschichten in der Regel mehrere hundert Nanometer dick und zeigen in Kombination mit darunter liegenden Schichten aus Glanz- oder Halbglanznickel einen sehr guten Glanz und eine hohe Korrosionsbeständigkeit [2]. Verfahren mit auf diese Anwendung hin optimierten Chromsäureelektrolyten sind seit vielen Jahrzehnten Stand der Technik bei der dekorativen Verchromung [3]. Die Verwendung von sechswertigen Chromverbindungen wird jedoch aufgrund ihrer Toxizität und Karzinogenität immer mehr eingeschränkt [4, 5]. So wurden in den 1970-er Jahren Abscheideverfahren auf Basis von dreiwertigen Chromsalzen als weniger schädliche Alternative zu Chromsäureelektrolyten in die Industrie eingeführt [6]. Die Reduktion von dreiwertigem Chrom in den Elektrolyten erfolgt in zwei Schritten:
Cr3+ + e- —> Cr2+ <Gl. 1>
Cr2+ + 2e- —> Cr0 <Gl. 2>
Üblicherweise werden dem Elektrolyten organische Substanzen zugesetzt, um die Effizienz der Reaktion gemäß Gleichung <2> zu erhöhen [7, 8]. Heute sind in Europa, Nordamerika und Ostasien zwar eine Vielzahl kommerziell erhältlicher Elektrolyte auf Basis von dreiwertigen Chromverbindungen verfügbar [9]. Allerdings erfüllen die technisch einsetzbaren Prozesse auf Basis der dreiwertigen Chromverbindungen die Anforderungen in Bezug auf die Optik nicht vollständig. Während Chrom aus einem Chrom(VI)elektrolyten ein bläuliches Aussehen besitzt, ist für die Schichten aus den meisten Chrom(III)elektrolyten ein leicht gelber oder dunkler Farbton charakteristisch [10]. Außerdem ist die Reproduzierbarkeit einer bestimmten Farbe nur bedingt möglich. Dies ist auf ein mangelndes grundlegendes Verständnis der Einflussfaktoren auf das optische Erscheinungsbild zurückzuführen. Neben ästhetischen Überlegungen sind diese Aspekte von entscheidender Bedeutung, wenn galvanisch verchromte Teile verschiedener Lieferanten gemeinsam verbaut werden. Ziel ist es, einen prozessstabilen Farbton im blauen Bereich des Farbspektrums zu erhalten, der dem Erscheinungsbild von Teilen aus Chrom(VI)elektrolyten möglichst nahekommt. Letztere gelten nach wie vor als Benchmark für die dekorative Verchromung [11].
In einer vorhergehenden Publikation der Autoren [12] wurde gezeigt, dass die Farbe der Chromschicht von der Morphologie der Oberfläche abhängt und durch geringe Mengen an Verunreinigungen beeinflusst wird. Bei der Abscheidung aus einem dreiwertigen Chromelektrolyten nehmen die Korngröße und die Rauheit während des Schichtwachstums zu. Dies führt zu einer Farbverschiebung von bläulich bei sehr geringer Dicke zu gelblich bei Dicken über 100 nm. Im Gegensatz dazu bleiben die Oberflächenmorphologie und das visuelle Erscheinungsbild bei Chromschichten aus sechswertigen Elektrolyten nahezu konstant.
Um ein bläuliches Aussehen für ein dreiwertiges System und gleichzeitig eine gute Beständigkeit der Beschichtung zu erzielen, muss eine feinkörnige Oberflächenstruktur für Schichtdicken von mehreren hundert Nanometern realisiert werden. Durch die Anwendung von gepulstem statt des sonst gebräuchlichen konstanten kathodischen Stroms kann das Kornwachstum aufgrund der periodischen Unterbrechung des Abscheidungsprozesses unterdrückt werden [13]. Mit dem Beginn jedes Stromimpulses erfolgt die Bildung von frischen Keimen, so dass in der Summe eine insgesamt feinkörnige Kristallstruktur vorliegt.
Puls- und Pulsumkehrbeschichtung wurden sowohl für die Abscheidung aus sechswertigen [14-16] als auch dreiwertigen [17-19] Systemen angewendet, meist bei Frequenzen zwischen 10 Hz und 10 kHz. Bei diesen Bedingungen wurde für die Chromabscheidung eine erhöhte Stromausbeute beobachtet. Dies wurde dadurch erklärt, dass während der Strompausen adsorbierter Wasserstoff von der Oberfläche entfernt wird und Chromionen an die Elektrodenoberfläche nachgeliefert werden können [20]. Dieser Effekt beeinflusst die Kornstruktur und Texturbildung der Chromschichten, was zu verbesserten mechanischen Eigenschaften [21] und einer höheren Korrosionsbeständigkeit führt [22]. Entsprechende Ansätze waren bisher vor allem darauf ausgerichtet, dickere Chromschichten für funktionelle Anwendungen herzustellen. Sie legten weniger Wert auf das optische Erscheinungsbild. Für die Anpassung der Farbe einer Chromoberfläche durch Verfeinern der Oberflächenmorphologie im Nanometerbereich, scheinen allerdings Pulsdauern und Ausschaltzeiten im Bereich von Sekunden günstig zu sein [23]. Ein neuerer Ansatz diskutiert die Anwendung der Niederfrequenz-Pulsbeschichtung mit Frequenzen von unter 1 Hz zur Verringerung der inneren Spannung von Chromschichten [24, 25].
Die Pulsabscheidung ist eine leistungsstarke Technik, bei der der Strom über verschiedene Parameter über einen weiten Bereich geändert werden kann. Für die vorliegende Arbeit wurden zwei verschiedene Pulsvarianten für die galvanische Abscheidung von Chrom aus einem dreiwertigen Elektrolyten ausgewählt. Die Ergebnisse werden mit Proben verglichen, die bei konstantem Strom aus der selben Lösung beschichtet wurden. Farbwerte wurden gemessen und REM-Bilder der Chromoberflächen aufgenommen, um das optische Erscheinungsbild und die morphologischen Eigenschaften der Schichten zu bewerten. Für das Niederfrequenz-Pulsregime wurden verschiedene Stadien des Schichtwachstums beobachtet, so dass Rückschlüsse auf die Keimbildung und das Wachstum von Chrom gezogen werden können. Die Ergebnisse der vorhergehenden Arbeit der Autoren über die Beziehungen von Farbe und Morphologie von galvanisch abgeschiedenen Chromschichten [12] wurden als Grundlage für die Interpretation der Ergebnisse herangezogen.
2 Experimentelles
2.1 Probenvorbereitung
Als Substrate wurden polierte Messingbleche (Größe 5 x 7,5 cm2) verwendet. Die Bleche wurden mit einem handelsüblichen alkalischen Elektrolytreiniger (HSO Uni 1, Herbert Schmidt GmbH, Solingen) entfettet. Dazu wurde über einen Zeitraum von 4 min eine kathodische Stromdichte von 2 A/dm2 angelegt. Als Anodenmaterial diente Edelstahl. Nach dem Entfetten wurden die Proben zur Aktivierung in 10-Vol.-%ige Schwefelsäure getaucht und mit 10 µm Nickel aus einem handelsüblichen hellen Nickelelektrolyten [26] beschichtet. In Tabelle 1 sind die Kenndaten des Nickelelektrolyten aufgeführt. Als Anodenkörper wurde schwefeldepolarisiertes Nickel verwendet.

Die Abscheidung von Chrom erfolgte aus einem handelsüblichen Elektrolyten auf Basis von Chrom(III)sulfat (SAPHIR 2000, Kiesow Dr. Brinkmann GmbH & Co. KG) bei pH 3,2 und einer Temperatur von 55 °C [27]. Die Abscheidung erfolgte in einem Becherglas mit zwei parallel angeordneten Metalloxidanoden (De Nora GreenChrome®). Während der Abscheidung wurden die Probenbleche parallel zu den Anoden mit einer Geschwindigkeit von 6 cm/s bewegt, um die Entfernung von anhaftenden Wasserstoffblasen von der Oberfläche zu unterstützen und den Massentransport zu erleichtern. Der gleiche Aufbau wurde sowohl für Abscheideversuche mit konstantem als auch mit gepulstem Strom verwendet. Für die Abscheidung mit Pulsstrom wurde ein BioLogic SP-150-Potentiostat mit VMP3B-20-Booster (20 A / 20 V) verwendet.
Die Chromabscheidung mittels Gleichstrom (DC) wurde bei 5 A/dm2 durchgeführt. Entsprechend dem praktisch anwendbaren Dickenspektrum von dekorativen Chromschichten [2] wurden etwa 500 nm als maximale Chromschichtdicke mit äquidistanten Zwischenschritten gewählt. Die Abscheidedauer wurde von 1 min bis 14 min variiert, entsprechend Schichtdicken von 40 nm bis 550 nm. Die Pulsabscheidungen wurden mit einer Pulsstromdichte von 5 A/dm2 durchgeführt. Bei höheren Stromdichten nimmt die Effizienz der Chromabscheidung aufgrund der Bildung von Chromhydroxiden in der Nähe der Elektrodenoberfläche schnell ab, so dass eine weitere Erhöhung der Pulsstromdichte nachteilig ist [28]. Es wurden zwei verschiedene Pulsvarianten verwendet. Für das Frequenzregime von 1 Hz wurde mit einer Einschaltzeit von 0,5 s und einer Ausschaltzeit von 0,5 s gearbeitet. Die Dauer der Beschichtung betrug 14 min. Die zweite, niederfrequente Pulsbeschichtung wurde mit einer Einschaltzeit von 15 s und einer Ausschaltzeit von 22,5 s durchgeführt. Die Abscheidungszeit wurde von 37,5 s (ein Puls) bis 15 min und 37,5 s (25 Pulse) variiert. Mit jeder gewählten Abscheidebedingung wurde eine Probe hergestellt.
2.2 Charakterisierung der Schichten
Die Farbmessungen wurden nach den Empfehlungen der International Commission on Illumination (CIE) [29] vorgenommen. Die Proben wurden mit sichtbarem Licht mit einem standardisierten D65-Spektrum bestrahlt. Das Spektrum des reflektierten Lichts wurde unter einem Winkel von 8° zur Senkrechten erfasst. Sowohl das gerichtete als auch das diffus reflektierte Licht wurden für die Analyse berücksichtigt. Es wurde ein Spektralphotometer CM-700d (Konica Minolta) mit einem Messfleck von 6 mm verwendet. Aus den gesammelten Spektraldaten wurden die Farbwerte im L*a*b*-System gemäß den ASTM-Richtlinien abgeleitet [30]. Pro Probe wurden zwölf Positionen unter gleichen Bedingungen vermessen und die Durchschnittswerte für jede Probe berechnet.
Die Dicke der Chromschichten wurde mittels Röntgenfluoreszenzspektroskopie (XRF) (Gerät: Fischerskop XDV) bei einer Spannung von 50 kV, einem Messfleck von 3 mm und einer Messzeit von 30 s pro Position bestimmt. Es wurden die selben Proben wie für die Farbmessungen untersucht. Die Dickenwerte wurden für jede Probe aus neun, gleichmäßig über die Oberfläche verteilten Positionen ermittelt und daraus ein Durchschnittswert berechnet.
Rasterelektronenmikroskopie (SEM) und elektronendispersive Röntgenspektroskopie (EDX) wurden mit einem SEM Hitachi S4800 mit Sekundärelektronendetektor bei einer Beschleunigungsspannung von 5 kV beziehungsweise 10 kV durchgeführt. Aus jeder Probe wurde ein Ausschnitt mit einer Fläche von etwa einem Quadratzentimeter für die Untersuchung mittels REM entnommen. Korngröße und Porendurchmesser wurden aus den mikroskopischen Aufnahmen gewonnen.
3 Ergebnisse und Diskussion
3.1 Abscheidung mit Gleichstrom (DC)
Die Farbwerte L*, a* und b* der mit Gleichstrom verchromten Proben sind in Abbildung 1 gegen die Dicke der Chromschicht aufgetragen. Der Parameter L* gibt die Helligkeit in einem Bereich von 0 (schwarz) bis 100 (weiß) an. a* und b* repräsentieren die Richtungen des Farbtons, wobei ein positiver Wert für a* als rot, ein negativer Wert für a* als grün, ein positiver Wert für b* als gelb und ein negativer Wert für b* als blaue Richtung des Farbtons zu sehen sind. Farblosigkeit entspricht a* = b* = 0. Für jeden Parameter wurde eine lineare Regression vorgenommen, um Tendenzen bei den Daten erkennen zu können (Tab. 2).

Abb. 1: Darstellung der Farbwerte L*, a* und b* als Funktion der Dicke der bei Gleichstrom (5 A/dm2) abgeschiedenen Chromschichten; angegeben sind die Trendlinien der linearen Regression, um Abhängigkeiten zwischen Farbwerten und Dicke aufzuzeigen

Das Verhältnis zwischen Farbe und Dicke entspricht qualitativ dem der früheren Arbeit der Autoren [12], das heißt mit abnehmender Dicke nimmt L* ab und b* zu. a* hängt nur gering von der Dicke der Chromschicht ab, wie aus dem niedrigen Korrelationskoeffizienten (R2 = 0,05) hervorgeht. Standardabweichungen liegen im erwarteten Bereich für die Farbmessung galvanisch abgeschiedener Chromschichten [10, 12]. Ein bläuliches Aussehen kann durch Gleichstrombeschichtung nur für Schichtdicken unter 100 nm erreicht werden, was für die meisten dekorativen Anwendungen ungeeignet ist.
Die Änderung der Werte für L* und b* wird durch eine Vergröberung der Oberflächenstruktur während des Schichtwachstums verursacht, was zu einer Zunahme der Korngröße und Rauheit führt. Wie aus den REM-Bildern (Abb. 2) ersichtlich ist, nimmt die durchschnittliche Korngröße von etwa 40 nm bei einer Schichtdicke von 40 nm auf 250 nm bei einer Schichtdicke von 550 nm zu. Alle Proben weisen Poren mit einem Durchmesser zwischen etwa 20 nm und bis zu 40 nm aufgrund der Wasserstoffentwicklung bei der Chromabscheidung auf.

Abb. 2: REM-Aufnahmen von Chromschichten, die bei Gleichstrom mit einer Stromdichte von 5 A/dm2 abgeschieden wurden, mit einer durchschnittlichen Schichtdicke von 40 nm (a), 230 nm (b) beziehungsweise 550 nm (c)

Die EDX-Analyse der Proben mit einer Chromschichtdicke von etwa 550 nm lässt geringe Mengen an Verunreinigungen in der Schicht erkennen (Tab. 3). Schwefel (ca. 2 Gew.%) und Kohlenstoff (ca. 1 Gew.%) sind sehr wahrscheinlich Abbauprodukte der organischen Elektrolytzusätze, wogegen Sauerstoff vermutlich Bestandteil von Oxiden ist, die beim Kontakt der Probe mit der Luft entstehen. Da die Elektrolytzusammensetzung für alle Versuche konstantgehalten wurde, kann von einer ähnlichen chemischen Zusammensetzung für alle Abscheideversuche ausgegangen werden. Die Verunreinigungen in den Schichten können einen leichten Einfluss auf ihr optisches Erscheinungsbild haben, dieses wird jedoch durch morphologische Effekte überlagert.
3.2 Pulsabscheidung mit 1 Hz Pulsfrequenz
Erste Versuche zur Pulsabscheidung wurden bei einer Frequenz von 1 Hz mit einer Ein- und Ausschaltzeit von jeweils 0,5 s durchgeführt. Dies entspricht einem Lastzyklus von 50 % der Gesamtdauer der Abscheidung. Die Berechnung der Pulsparameter erfolgte nach den Gleichungen <3> und <4> :
ƒ = 1/T = 1/(ton + toff) <3>
Θ = ton∕T = ton ∗ ƒ <4>
mit: ƒ – Frequenz
T – Periodendauer
ton – On-Zeit
toff – Off-Zeit
Θ – Lastzyklus
Mit den aufgeführten Bedingungen wurde eine durchschnittliche Dicke der Chromschicht von 290 nm abgeschieden. Die Oberflächenmorphologie der Chromschicht (Abb. 3) unterscheidet sich stark von der mittels Gleichstrom abgeschiedenen Schicht. Anstelle einer kugelförmigen Struktur weisen die Körner eine dreieckige oder polygonale Form mit Größen zwischen 50 nm und 150 nm auf. Die Korngrenzen sind jedoch im Vergleich zur Schicht der Gleichstromabscheidung viel schwerer zu erkennen. Außerdem sind Anzahl und Durchmesser der Poren der Schichten aus der Pulsabscheidung größer, als die der Schichten aus der Gleichstromabscheidung. Eine ausgeprägt hohe Porosität verschlechtert die Korrosionsbeständigkeit sowie das optische Erscheinungsbild der Chromschicht. Der Vergleich mit den Farbwerten einer Schicht aus der Gleichstromabscheidung mit der gleichen Dicke zeigt eine Abnahme des L*-Werts von ungefähr 82,5 auf 79,9 und eine Zunahme des b*-Werts von +0,5 auf +1,6; dies entspricht einem dunkleren und gelblicheren Farbton.

Abb. 3: REM-Aufnahme einer Chromschicht, die mit gepulstem Strom mit einer Pulsstromdichte von 5 A/dm2, einer Frequenz von 1 Hz und einem Lastzyklus von 50 % abgeschieden wurde
3.3 Wachstum der Chromschicht
Der Grund für die Bildung der oben diskutierten Strukturen liegt in der Bildung und dem Wachstum von Chromkeimen während der galvanischen Abscheidung. Abbildung 4 zeigt schematisch die Bildung einer Chromschicht auf einem glatten Metallsubstrat bei der Verwendung eines dreiwertigen Chromelektrolyten. Im Anfangsstadium bildet sich an der Elektrodenoberfläche eine hohe Anzahl von Chromkeimen (Abb. 4a). Mit zunehmender Abscheidezeit sinkt die Keimbildungsrate, während das Wachstum der Keime fortschreitet, was zu einem globularen Wachstumstyp führt (Abb. 4b). Aufgrund der geringen Abscheidungsrate bei der Chromabscheidung werden einige Sekunden benötigt, um eine kompakte Schicht zu bilden (Abb. 4c). Im Falle der Pulsabscheidung bei Frequenzen von 1 Hz und höher wird das Wachstum in einem frühen Stadium gestoppt, lange bevor sich eine kompakte Schicht bilden kann. Dies führt zu einer polygonalen Morphologie mit hoher Porosität (Abb. 3). Doppelschichtlade- und Entladungsprozesse beeinflussen ebenfalls den Abscheidungsprozess bei der Pulsabscheidung mit hohen Frequenzen, da sie die Stromwellenform verzerren können [13]. Daher scheint die Abscheidung einer kompakten Chromschicht während eines Strompulses für die Oberflächeneigenschaften der Schicht vorteilhaft zu sein. Aus diesem Grund wird beim Pulsen eine On-Zeit von mehreren Sekunden benötigt.

Fig. 4 Schematische Darstellung des Chromschichtwachstums während der galvanischen Abscheidung; die Phasen (a–c) verdeutlichen die frühen Stadien der Schichtbildung, (d) zeigt das weitere Wachstum bei konstantem Strom und (e) das schichtweise Wachstum bei Anwendung eines niederfrequenten gepulsten Stroms
Beim weiteren Wachstum nach der Bildung einer kompakten Schicht überlappen sich die Konzentrationsgradienten um die Keime, so dass einige Keime auf Kosten anderer wachsen (Abb. 4d). Dies führt zu einer Zunahme der Korngröße und Rauheit und damit zu einer Farbverschiebung. Solche Effekte treten bei Gleichstrombeschichtung auf.
Wenn dagegen der Strom unterbrochen wird, reduzieren sich die vorhandenen Konzentrationsgradienten und die Verhältnisse für eine erhöhte Keimbildung liegen wieder vor. Sobald der Strom wieder eingeschaltet wird, kann der Prozess aus Keimbildung und Keimwachstum erneut beginnen. Ein derartiges Stromregime würde einer Pulsabscheidung mit Frequenzen weit unter 1 Hz entsprechen. Unter der Annahme, dass der Keimbildungsmechanismus bei jedem Stromimpuls reproduzierbar ist, kann sich Schicht für Schicht eine neue Struktur bilden (Abb. 4e). Die Morphologie der finalen Oberfläche sollte mit der Beschaffenheit jeder einzelnen Lage vergleichbar sein, sodass das optische Erscheinungsbild weitgehend unabhängig von der Gesamtschichtdicke ist.
3.4 Pulsabscheidung mit niedriger Frequenz
Zur Prüfung der getroffenen Annahmen wurde eine niederfrequente Pulsabscheidung mit einer Einschaltzeit von 15 s und einer Ausschaltzeit von 22,5 s durchgeführt, was einer Frequenz von 0,027 Hz und einem Lastzyklus von 40 % entspricht. Die Pulsstromdichte wurde mit 5 A/dm2 beibehalten. Die Gesamtabscheidezeit, also die Anzahl der Impulse, wurde variiert; anschließend wurden die Farbwerte und die Schichtdicke gemessen.
Für die niederfrequente Impulsbeschichtung wird die Abscheidezeit als Anzahl der Impulse angegeben, da diese Bezeichnung besser geeignet ist, die Anzahl der abgeschiedenen Einzelschichten darzustellen. Die Dicke nimmt linear mit der Anzahl der Impulse zu (Abb. 5), was dem vorgeschlagenen Modell entspricht. Wie im Fall der Abscheidung mit Gleichstrom wurden die Werte für L* und b* gegen die Schichtdicke aufgetragen (Abb. 6). Die Standardabweichung der Farbwerte ist vergleichbar mit der unter Gleichstrombedingungen. Mehrere Proben wurden im REM untersucht (Abb. 7). Zunächst sind die Ergebnisse für das unbeschichtete Glanznickelsubstrat gezeigt, die einer Chromschichtdicke von Null entsprechen. Da Nickel eine stark gelbliche Farbe hat, liegt der b*-Wert im hohen positiven Bereich (+6,7), während der Wert für L* im gleichen Bereich (83,0) wie bei Chrom aus einer Gleichstromabscheidung liegt. Die Morphologie von Glanznickel ist sehr feinkörnig, hat jedoch eine andere Textur als Chrom (Abb. 7a).

Abb. 5: Auftragung der Schichtdicke gegen die Anzahl der Pulse für Chromschichten, die mit gepulstem Strom (Pulsstromdichte 5 A/dm2, Frequenz 0,027 Hz, Lastzyklus 40 %) abgeschieden wurden

Abb. 6: Farbwerte L* und b* als Funktion der Dicke der Chromschichten, die bei gepulstem Strom mit einer Pulsstromdichte von 5 A/dm2, einer Frequenz von 0,027 Hz und einem Lastzyklus von 40 % hergestellt wurden; die roten Datenpunkte bei einer Dicke von Null entsprechen der Glanznickelschicht des Substrats

Abb. 7: REM-Aufnahmen der Glanznickelschicht und von Chromschichten, die mit gepulstem Strom mit einer Pulsstromdichte von 5 A/dm2, einer Frequenz von 0,027 Hz und einem Lastzyklus von 40 % abgeschieden wurden; Glanznickel ohne Chrom (a), Chromschicht nach einem Puls ((b), 5 nm bis 10 nm Chrom), nach 5 Pulsen ((c), 40 nm Chrom), nach 15 Pulsen ((d), 95 nm Chrom) und nach 25 Pulsen ((e), 210 nm Chrom)
Durch die Beaufschlagung der Probe mit einem einzelnen Puls werden etwa 5 nm bis 10 nm Chrom abgeschieden, wobei b* zu einem niedrigeren Wert (+2,5) verschoben wird, während L* abnimmt (80,1). Da die Dicke der Chromschicht sehr gering ist, tragen sowohl das Nickelsubstrat als auch die Chromdeckschicht zum optischen Gesamterscheinungsbild bei. Darüber hinaus ist die Chromschicht möglicherweise nicht vollständig geschlossen, so dass ein Teil der Nickeloberfläche noch offen liegt. Die Morphologie ist Glanznickel sehr ähnlich (Abb. 7b), da die Kristallstruktur des Nickels von Chrom repliziert wird – dieser Effekt tritt in der Regel bei der galvanischen Metallabscheidung in der Anfangsphase der Abscheidung grundsätzlich auf – und sich die typische Chrommorphologie noch nicht gebildet hat. Nach fünf Impulsen, die einer Dicke von 40 nm entsprechen, wird b* auf negative Werte verschoben, was auf einen bläulichen Farbton hinweist. L* wird auf 83,9 erhöht, ein Helligkeitswert, der sogar höher ist als der L*-Wert der Chromoberfläche der hergestellten Proben aus einer Abscheidung mit Gleichstrom. Hier hat sich eine Morphologie gebildet, die der Chromschicht aus der Gleichstromabscheidung mit der gleichen Dicke ähnlich ist (Abb. 2a bzw. 7c). Die Porosität ist ebenfalls so gering wie bei den unter konstantem Strom hergestellten Proben. Die Korngröße beträgt etwa 40 nm.
Wenn die Anzahl der Impulse und damit die Dicke der Chromschicht weiter erhöht wird, bleiben L* und b* nahezu stabil, während sich die Morphologie ändert (Abb. 7d). Optimale Farbwerte von L* = 84,0 und b* = -0,5 konnten erreicht werden. Bei 25 Pulsen, entsprechend einer Dicke von 210 nm, stieg die Korngröße auf Werte zwischen 70 nm und 100 nm an (Abb. 7e). Somit ist die Oberflächenmorphologie immer noch nicht völlig unabhängig von der Dicke der Chromschicht. Die Farbwerte sind geringfügig auf L* = 83,6 und b* = -0,3 verschoben, allerdings verbleibt b* damit immer noch im negativen Bereich. Eine durch Gleichstromabscheidung hergestellte Chromschicht mit ähnlicher Dicke, wie in Abbildung 1 zu sehen ist, zeigt Farbwerte von etwa L = 82,5 und b = + 0,3. Das optische Erscheinungsbild der Chromschicht wurde durch die Anwendung von Pulsstrom erheblich verbessert, indem der Farbton von gelblich nach bläulich verschoben und die Helligkeit erhöht wurde.
3.5 Kombination aus Gleichstrom- und Pulsstromabscheidung
Wie dargelegt wurde, kann eine Verbesserung des Aussehens durch niederfrequente Pulsabscheidung erreicht werden. Das Verfahren ist jedoch sehr zeitaufwändig. Im Vergleich zu einem Prozess unter Einsatz von Gleichstrom verlängert sich die Beschichtungszeit für die Pulsabscheidung um den Faktor 2,5. Für die Abscheidung einer Chromschicht mit einer Dicke von ungefähr 220 nm werden bei konstantem Strom etwa 6 min und 15 s und bei gepulstem Strom 25 Impulse beziehungsweise 15 min und 37,5 s benötigt (Abb. 8a, b).

Abb. 8: Stromregime für die galvanische Abscheidung von etwa 220 nm Chrom mit konstantem Strom (a), gepulster Strom mit einer Frequenz von 0,027 Hz und einem Lastzyklus von 40 % (b) sowie eine Kombination aus beiden (c)
Die Gesamtbeschichtungszeit lässt sich durch Kombination von Gleichstrom- und Pulsstrom reduzieren (Abb. 8c). Dazu werden im ersten Schritt durch Anwendung von Gleichstrom in 5 min mit einer Stromdichte von 5 A/dm2 etwa 180 nm Chrom abgeschieden, was etwa 80 % der hier angestrebten endgültigen Schichtdicke entspricht. Anschließend werden 5 Pulse (3 min und 7,5 s) durch niederfrequente Pulsbeschichtung mit den oben genannten Parametern hinzugefügt.
Auf diese Weise werden fünf dünne Lagen mit feinkörniger Struktur auf eine dicke Basisschicht aufgebracht. Die Gesamtbeschichtungszeit beträgt in diesem Fall etwa 8 min. Mit dieser Methode werden Farbwerte von L* = 83,7 und b* = -0,5 erreicht. Die Morphologie der Chromschicht (Abb. 9) ist der Oberflächenstruktur einer mit 25 Pulsen der niederfrequenten Pulsabscheidung hergestellten Beschichtung (Abb. 7e) sehr ähnlich. Die Korngröße (70 nm–100 nm) und die Porosität sind gleich. Die durchschnittliche Dicke der Vergleichsproben liegt zudem nahe beieinander. Durch das kombinierte Pulsregime werden etwa 220 nm Chrom und durch 25 Pulszyklen 210 nm abgeschieden. Somit lassen sich sehr ähnliche Ergebnisse erzielen, indem eine Kombination aus Gleichstrom und Pulsstrom oder eine reine Pulsstrom-Abscheidung angewendet wird.

Abb. 9: REM-Aufnahmen einer Chromschicht, die in einem kombinierten Prozess (Abb. 8c) aus konstantem Strom bei einer Stromdichte von 5 A/dm2 und gepulstem Strom mit einer Pulsstromdichte von 5 A/dm2 und einer Frequenz von 0,027 Hz abgeschieden wurde (entsprechend einem Lastzyklus von 40 %)
4 Schlussfolgerungen
Die Pulsabscheidung ist geeignet, um Chrom aus einem Elektrolyten auf Basis von dreiwertigem Chrom (Chromsulfat) mit einem maßgeschneiderten optischen Erscheinungsbild herzustellen. Bei Einsatz eines konstanten Stroms nimmt die Korngröße der Chromschicht während der Abscheidung zu, was zu einer Farbverschiebung von bläulich nach gelblich führt. Eine niederfrequente Pulsbeschichtung mit einer Pulsstromdichte von 5 A/dm2 mit einer Einschaltzeit von 15 s und einer Ausschaltzeit von 22,5 s ist für die Schichtqualität vorteilhaft. Auf diese Weise können Chromschichten mit einem bläulichen Farbton und hoher Helligkeit sowie mit Dicken von mehr als 200 nm erzeugt werden. Optimale Farbwerte von L* = 84,0 und b* = -0,5 wurden nach einer Abscheidezeit von 9 min und 22,5 s (15 Zyklen) erreicht. Eine Kombination aus konstantem und gepulstem Strom führt zu ähnlichen Ergebnissen in Bezug auf Morphologie und Farbwerte wie die Verwendung von reinem Pulsstrom, jedoch bei derHälfte der Prozesszeit. Zukünftige Arbeiten werden auf eine detaillierte Untersuchung der Pulsparameter und der Mikrostruktur der Schichten abzielen .
Danksagung
Open-Access-Finanzierung durch Projekt DEAL. Diese Forschung wurde im Rahmen einer Zusammenarbeit zwischen der Technischen Universität Ilmenau und der Hansgrohe SE durchgeführt. Der Kiesow Dr. Brinkmann GmbH & Co. KG wird für die Bereitstellung der Nickel- und Chromelektrolyte gedankt.
Literatur
[1] J. H. Lindsay: Decorative and hard chromium plating; Plat Surf Finish 84 (1997) 8, S. 50–51
[2] D. L. Snyder: Decorative chromium plating basics; Met Finish 110 (2012) 2, S. 14–21
[3] S. L. Handy, C. F. Oduoza, T. Pearson T (2006) Theoretical aspects of electrodeposition of decorative chromium from trivalent electrolytes and corrosion rate study of different nickel/chromium coatings; Trans IMF 84 (2006) 6, S. 300–308; https://doi.org/10.1179/174591906x162946
[4] European Chemicals Agency Authorisation List, EC No. 215– 607–8, 231–801–5, 231–889–5, 231–906–6, 232–140–5, 232– 143–1, 234–190–3, 236–881–5
[5] V. K. Gupta, A. K. Shrivastava, N. Jain: N (2001) Biosorption of chromium(VI) from aqueous solutions by green algae Spirogyra species; Water Res 35 (2001) 17, S. :4079–4085; https://doi.org/10.1016/S0043-1354(01)00138-5
[6] L. Gianelos: Production experience with trivalent chromium plating solutions; Plat Surf Finish 66 (1979) 5, S. 56–60
[7] D. Del Pianta, J. Frayret, C. Gleyzes, C. Cugnet, J. C. Dupin, I. Le Hecho: Determination of the chromium(III) reduction mechanism during chromium electroplating. Electrochim Acta 284 (2018), S. 234–241; https://doi.org/10.1016/j.electacta.2018.07.114
[8] R. Katirci: A chrome coating from a trivalent chromium bath containing extremely low concentration of Cr3+ ions; Int J Surf Sci Eng 10 (2016) 1, S. 73–85
[9] Z. X. Zeng, A. M Liang, J. Y. Zhang: A review of recent patents on trivalent chromium plating;Recent Pat Mater Sci 2 (2009) 1, S. 50–57
[10] D. L. Snyder: Distinguishing trivalent chromium deposits by color; Plat Surf Finish 90 (2003) 11, S. 34–39
[11] Y. Sheasha, D. Yücel, L. A. Kibler, M. Knape, S. Holl, S. Henne, S. Heitmüller, T. Jacob: Potentiodynamic chromium deposition from trivalent and hexavalent systems on glassy carbon elec- trodes: initial stages and mechanistic insights; ChemElectroChem 4 (2017) 6, S. 1390–1394. https://doi.org/10.1002/celc.201700175
[12] M. Leimbach, C. Tschaar, D. Zapf, M. Kurniawan, U. Schmidt, A. Bund: Relation between color and surface morphology of electrodeposited chromium for decorative applications; J Electrochem Soc 166 (2019) 6, S. D205–D211; https://doi.org/10.1149/2.0871906jes
[13] W. E. G. Hansal, S. Roy: Pulse plating; Eugen G. Leuze Verlag KG, Bad Saulgau, (2012), S. 72–82; https://doi.org/10.12850/9783874803236.004
[14] D. T. Chin, H. B. Zhang: HB () A study of pulse pulse plating of chromium; Electrochim Acta 31 (1986) 3, S. 299–306; https://doi. org/10.1016/0013-4686(86)80082-2
[15] P. Leisner, G. Bechnielsen, P. Moller: Current efficiency and crystallization mechanism in pulse plating of hard chromium; J Appl Electrochem 23 (1993) 12, S. 1232–1236
[16] J. H. Chang, F. Y. Hsu, M. J. Liao, C. A. Huang: A study of direct- and pulse-current chromium electroplating on rotating cylinder electrode (RCE); Appl Surf Sci 253 (2007) 16, S. 6829–6834; https://doi.org/10.1016/j.apsusc.2007.01.124
[17] Z. M. Tu, Z. O. Yang, J. H. Zhang: Pulse plating with a trivalent chromium plating bath; Plat Surf Finish 77 (1990) 10, S. 55–57
[18] S. Mohan, G. Saravanan, N. G. Renganathan: Comparison of chromium coatings and electrochemical behaviour with direct current and pulse current deposition in trivalent chromium formate urea bath as alternative to conventional Cr coatings; Surf Eng 27 (2011) 10, S. 775–783; https://doi.org/10.1179/174329408x32633 5
[19] F. I. Danilov, V. S. Protsenko, V. O. Gordiienko, A. S. Baskevich, V. V. Artemchuk: Electrodeposition of nanocrystalline chromium-carbon alloys from electrolyte based on trivalent chromium sulfate using pulsed current; Prot Met Phys Chem 48 (2012) 3, S. 328–333. https://doi.org/10.1134/S2070205112030057
[20] A. Lozano-Morales, R. Renz, J. Fortman, E. J. Taylor: Electrically mediated process for functional and decorative trivalent chromium electroplating: an alternative to hexavalent chromium; ECS Trans 6 (2007) 9, S. 51–61. https://doi.org/10.1149/1.2790401
[21] V. S. Protsenko, F. I. Danilov, V. O. Gordiienko, A. S. Baskevich, V. V. Artemchuk: Improving hardness and tribological characteristics of nanocrystalline Cr-C films obtained from Cr(III) plating bath using pulsed electrodeposition; Int J Refract Met H 31 (2012), S. 281– 283; https://doi.org/10.1016/j.ijrmhm.2011.10.006
[22] G. Saravanan, S. Mohan: Corrosion behavior of Cr electrodeposited from Cr(VI) and Cr(III)-baths using direct (DCD) and pulse electrodeposition (PED) techniques. Corros Sci 51 (2009) 1, S. 197–202; https://doi.org/10.1016/j.corsci.2008.10.005
[23] R. Giovanardi, A. Bozza: Effect of temperature on pulsed current chromium electrodeposition from Cr(III) aqueous solutions; Metall Ital 106 (2014) 7–8, S. 9–16
[24] S. R. Brankovic: Crack formation during electrodeposition and post-deposition aging of thin film coatings; NASF Surf Technol White Papers 83 (2019) 5, S. 8–16
[25] T. D. Hall, J. Xu, R. Radhakrishnan, St. T. Snyder, E. J. Taylor, M. E. Inman, M. Feathers, M. Johnson: Improved wear performance of REACH compliant trivalent chromium plating process; Paper presented at SUR/FIN, Rosemont, IL (2019)
[26] Kiesow Dr. Brinkmann GmbH & Co. KG (2017), Data Sheet ORION 4000 Bright Nickel Electrolyte
[27] Kiesow Dr. Brinkmann GmbH & Co. KG (2015) Data Sheet SAPHIR 2000 Bright Chromium Electrolyte
[28] M. Leimbach, C. Tschaar, U. Schmidt, A. Bund: Electrochemical characterization of chromium deposition from trivalent solutions for decorative applications by EQCM and near-surface pH measurements; Electrochim Acta 270 (2018), S. 104–109. https://doi.org/10.1016/j.electacta.2018.03.011
[29] CIE Technical Report No. 15 (2004) Colorimetry, 3rd ed.
[30] ASTM E 308-01, Standard Practice for Computing the Colors of Objects by Using the CIE System
DOI: 10.7395/2020/Leimbach1
Hinweis zur Erstveröffentlichung – Open Access
Dieser Artikel unterliegt den Bestimmungen einer Creative Commons Attribution 4.0 International License, die die Verwendung, Weitergabe, Anpassung, Verteilung und Reproduktion in jedem Medium oder Format ermöglicht, sofern Sie dem/den ursprünglichen Autor(en) die entsprechende Anerkennung geben und der Quelle einen Link zur Creative Commons-Lizenz bereitstellen und angeben, ob Änderungen vorgenommen wurden. Die Bilder oder anderes Material von Drittanbietern in diesem Artikel sind in der Creative Commons-Lizenz des Artikels enthalten, sofern in einer Kreditlinie für das Material nichts anderes angegeben ist. Wenn das Material nicht in der Creative Commons-Lizenz des Artikels enthalten ist und Ihre beabsichtigte Verwendung nicht gesetzlich vorgeschrieben ist oder die zulässige Verwendung überschreitet, müssen Sie die Genehmigung direkt vom Inhaber des Urheberrechts einholen. Eine Kopie dieser Lizenz ist zu finden unter
http://creativecommons.org/licenses/by/4.0/.
1) Fachgebiet Elektrochemie und Galvanotechnik, Technische Universität Ilmenau, Gustav-Kirchhoff-Straße 6,
D-98693 Ilmenau
2) Hansgrohe SE, Auestraße 5-9, D-77761 Schiltach