Der Zufall spielt in chemischen Reaktionen oft eine große Rolle. Fast immer entstehen dabei zahlreiche unerwünschte Nebenprodukte, die unnötig Energie und Ressourcen verbrauchen. Ein Forschungsteam um Professorin Swetlana Schauermann vom Institut für Physikalische Chemie der Christian-Albrechts-Universität zu Kiel (CAU) kombiniert verschiedene Messverfahren, um chemische Reaktionen auf atomarer Ebene zu untersuchen und so grundlegend besser zu verstehen. In der renommierten Fachzeitschrift Angewandte Chemie haben sie jetzt eine Methode vorgestellt, mit der sich Reaktionen so gestalten lassen, dass am Ende nur das gewünschte Molekül entsteht. Den Unterschied macht eine spezielle Extraschicht von Molekülen, die als Katalysator die gewünschte Reaktion gezielt auslöst.

Mit hochpräzisen Messmethoden will das Forschungsteam um Prof. Swetlana Schauermann (v. r.), Carsten Schröder und Marvin Schmidt chemische Reaktionen auf atomarer Ebene verstehen, um sie zielgerichtet ablaufen zu lassen (© Julia Siekmann, Uni Kiel)
Was genau dazu führt, dass am Ende einer chemischen Reaktion ein bestimmter neuer Stoff entsteht, ist im Einzelnen nicht bekannt. Die Synthese von neuen Molekülen läuft häufig nach dem Trial and error-Prinzip ab: Wissenschaftlerinnen und Wissenschaftler müssen oft zahlreiche Tests durchführen, bis sie das gewünschte Ergebnis erhalten. Das Kieler Forschungsteam verfolgt einen anderen Ansatz und kombinierte dafür spezielle spektroskopische und mikroskopische Methoden. Wir wollen zunächst die Prozesse auf atomarer Ebene verstehen, um anschließend selektive Katalysatoren entwickeln zu können, mit denen sich chemische Produkte gezielt herstellen lassen, sagt Swetlana Schauermann, Professorin für Oberflächenchemie und Katalyse an der CAU.
Aufgrund seiner bisherigen Untersuchungen nahm das Team an, dass eine zusätzliche Molekülschicht auf Oberflächen eine gezielte Reaktion auslösen kann. Dafür untersuchten sie, wie aus Acrolein mithilfe eines Palladiumkatalysators gezielt Propenol hergestellt werden kann, wenn die Oberfläche des Metalls vorab mit Allylcyanid beschichtet wurde. Normalerweise kann durch eine Reaktion mit Wasserstoff, auch Hydrierung genannt, entweder Propenol (Alkohol), oder Propanal (Aldehyd) entstehen.

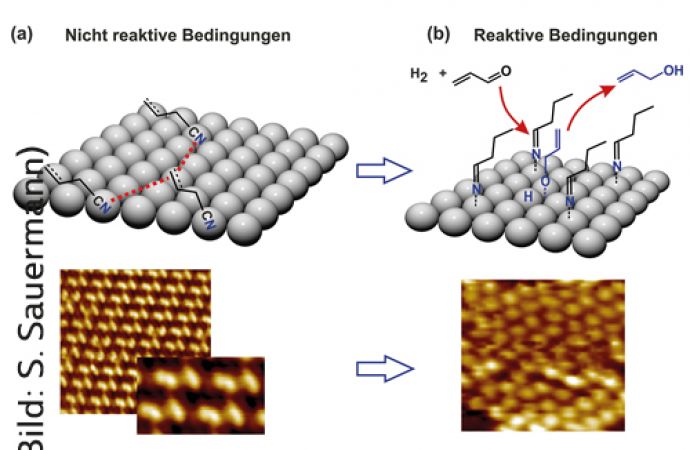
Unter dem Rastertunnelmikroskop konnten die Chemikerinnen und Chemiker sehen, wie sich die Moleküle auf der Oberfläche ihres Katalysatormetalls im nicht-reaktiven Zustand (a) und unter reaktiven Bedingungen (b) unterscheiden. Das Modell zeigt, wie sich die chemische Zusammensetzung der Ligandenlage unter reaktiven Bedingungen verändert und so die Entstehung von Propenol begünstigt (© Swetlana Schauermann)
Als Molekül für die zusätzliche Schicht hat die Forschenden Allylcyanid gewählt, weil es eine spezielle elektronische Struktur und eine hohe Elektronendichte besitzt. Aufgrund seiner Eigenschaften kann es sehr gut mit reagierenden Molekülen in Wechselwirkungen treten, erklärt Carsten Schröder, Doktorand in der Arbeitsgruppe von Schauermann und Erstautor der Studie. Außerdem spielt es in zahlreichen Industriezweigen eine Rolle, in denen mit organischen Synthesen gearbeitet wird.
Für seine Experimente beschichtete das Forschungsteam zunächst reines Palladiummetall mit Allylcyanid. Im Rastertunnelmikroskop konnten sie eine Schicht im Detail sichtbar machen und zeigen, dass die drei Kohlenstoffatome des Allyls flach auf den Metallatomen lagen. Als sie die Oberfläche anschließend Wasserstoff aussetzten, begann eine chemische Umwandlung und die flache Schicht veränderte sich. Im Rastertunnelmikroskop zeigten sich jetzt deutlich kürzere Abstände zwischen den Allylcyanidmolekülen.
Durch eine Kombination ihrer spektroskopischen und mikroskopischen Analysemethoden fanden die Forschenden heraus, was passiert war: Der Wasserstoff hatte sich an das Allylcyanidmolekül gebunden und es in einen gesättigten Kohlenwasserstoff mit einer sogenannten Iminfunktion umgewandelt, sagt Schröder. Die Molekülenden mit dem gesättigten Kohlenwasserstoffrest verloren den Kontakt zu den Palladiumatomen, wodurch sich die Moleküle aufrichteten und so eine dichtere Schicht auf der Oberfläche bildeten. Hierauf konnte das Acrolein jetzt positionsgenau andocken und so den Hydrierungsprozess auslösen, der zur Entstehung von Propenol führt.

An der Infrarotspektroskopieanlage stellt Doktorand Carsten Schröder den Druck der Acrolein-Moleküle ein, um die chemische Reaktion zu starten (© Julia Siekmann, Uni Kiel)

Marvin Schmidt führt Proben des Katalysatormetalls ins Rastertunnelmikroskop ein, um atomare Veränderungen auf der Oberfläche zu untersuchen (© Julia Siekmann, Uni Kiel)
In dieser Art ist es nach Mitteilung des CAU zum ersten Mal gelungen, einen Katalysator mit einer zusätzlichen Molekülschicht zu aktivieren und auf atomarer Ebene zu untersuchen. Ein detailliertes Verständnis solcher Prozesse könnte nach Aussage von Schauermann das Forschungsgebiet zu Katalysatoren rasant weiterentwickeln. Überflüssige Reaktionsprodukte zu entfernen und zu entsorgen, ist bislang mit viel Aufwand verbunden. Wenn wir in der Lage sind, einzelne Moleküle gezielt herzustellen, können wir Energie, Kosten und Ressourcen sparen und zum Beispiel zu umweltfreundlicheren Prozessen beitragen.J. Siekmann
Kontakt:
Prof. Dr. rer. nat. Swetlana Schauermann, E-Mail: schauermann@pctc.uni-kiel.de
Originalpublikation:
C. Schröder, M. C. Schmidt, Ph. A. Haugg, A.-K. Baumann, J. Smyczek, S. Schauermann: Understanding Ligand-Directed Heterogeneous Catalysis: When the Dynamically Changing Nature of the Ligand Layer Controls the Hydrogenation Selectivity; Angew. Chem. Int. Ed. 2021, 60, https://doi.org/10.1002/anie.202103960
- www.uni-kiel.de