Die anodische Auflösung von Aluminium in Lewis-sauren ionischen Flüssigkeiten, bestehend aus Aluminiumchlorid und 1-Ethyl-3-methylimidazoliumchlorid, wurde mittels linearer Polarisation und zyklischer Voltammetrie, der elektrochemischen Quarzkristall-Mikrowaage (EQCM) und Chronopotentiometrie bei Umgebungstemperatur untersucht. In einem 2:1-Elektrolyten wurde eine anodische Passivierung der Arbeitselektrode beobachtet, während in einem 1,5:1-Elektrolyten keine Passivierung auftrat. Die Chronopotentiometrie belegt, dass die Passivierung durch eine lokale Verfestigung des Elektrolyten aufgrund einer Erhöhung der Aluminiumkonzentration in der Nähe der Anode verursacht wird. EQCM-Daten unterstützen diese Ergebnisse.
Anodic dissolution of aluminum and anodic passivation in [EMIm]Cl-based ionic liquids
The anodic dissolution of aluminum in Lewis acidic ionic liquids consisting of AlCl3 and 1-ethyl-3-methylimi-dazolium chloride was studied using linear sweep and cyclic voltammetry, an electrochemical quartz crystal microbalance (EQCM) and chronopotentiometry at ambient temperature. Anodic passivation of the working electrode was observed in a 2:1 electrolyte while no passivation was found in a 1.5:1 electrolyte. Chronopotentiometry proves the passivation to be caused by local solidification of the electrolyte due to an increase in the aluminum concentration near the anode. EQCM data support these results.
1 Einleitung
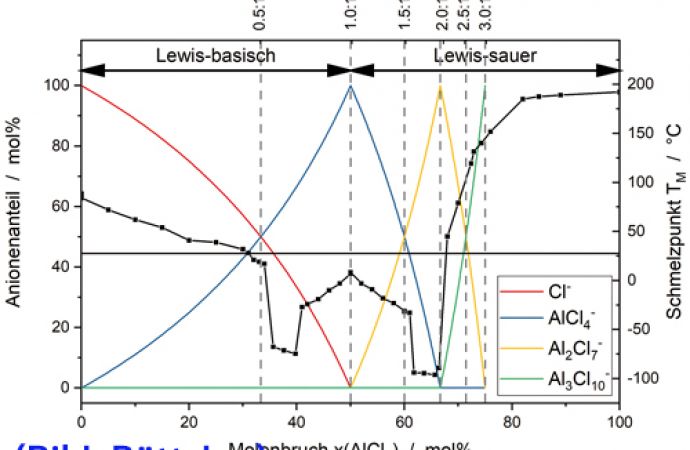
Elektrochemisch abgeschiedenes Aluminium beziehungsweise Aluminiumlegierungen stellen sehr interessante Beschichtungen dar. Vor allem die Abscheidung aus ionischen Flüssigkeiten hat sich als erfolgversprechend herausgestellt [1]. Mischungen aus Aluminiumchlorid (AlCl3) mit Salzen auf Basis von Imidaozolium, beispielsweise 1-Ethyl-3- methylimidazolchlorid ([EMIm]Cl), wurden intensiv untersucht. Die Elektrolyte zeigen eine gute Löslichkeit für unterschiedliche Metallsalze, was die Abscheidung von Aluminium und zahlreichen Aluminiumlegierungen erlaubt [2–5]. Die Lewis-Azidität der Schmelze kann über eine Änderung des